Microscopia elettronica a singole molecole
Panoramica
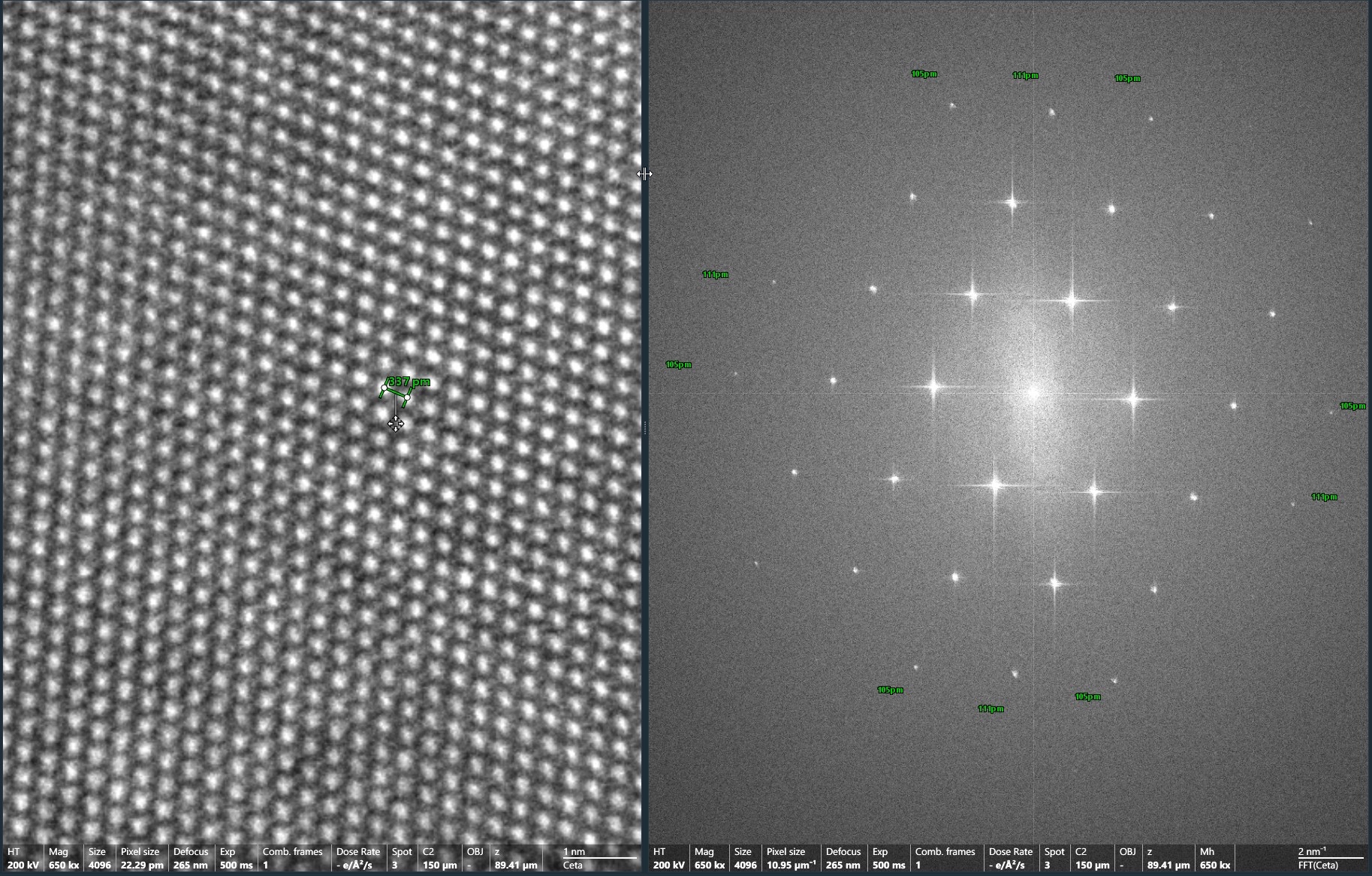
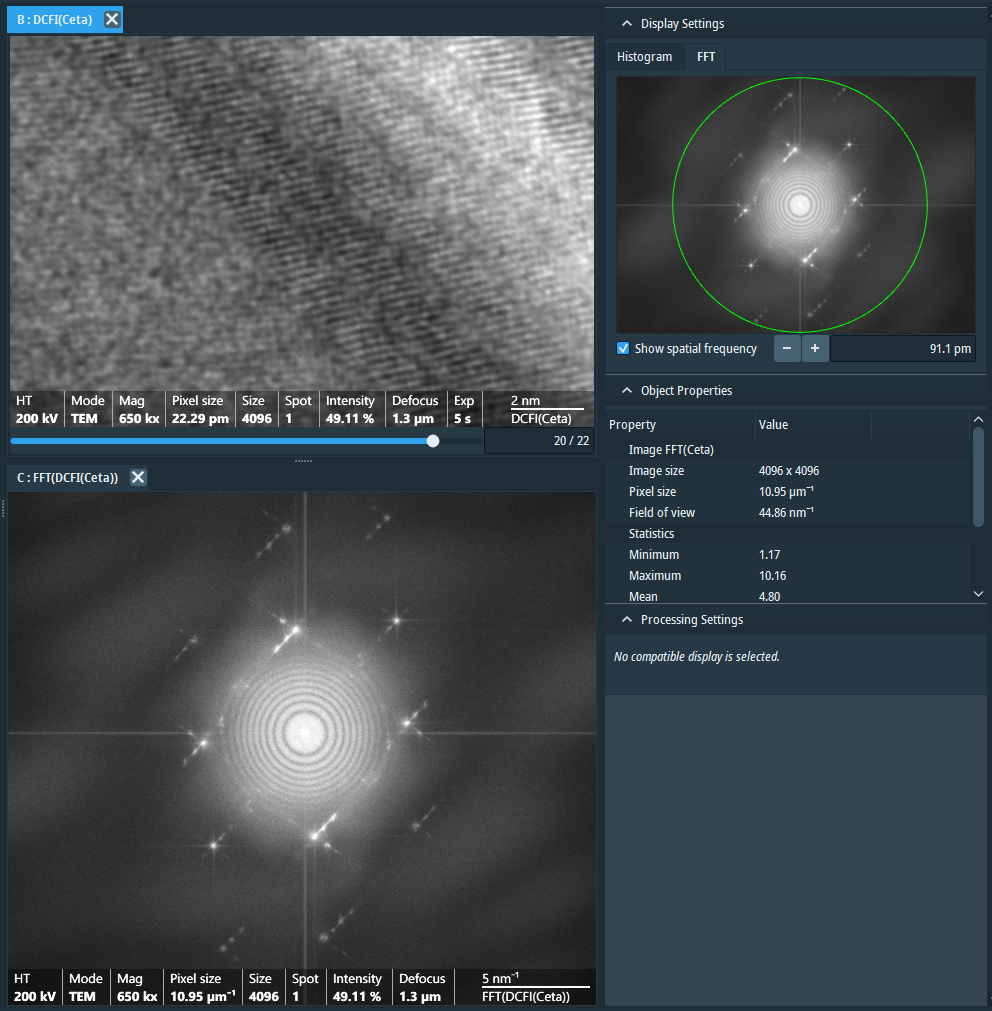
La piattaforma Electron Microscopy Single Molecules (EMSM) di IFOM è specializzata nella visualizzazione di acidi nucleici e proteine tramite tecniche di microscopia elettronica a trasmissione (TEM) ad alta risoluzione e a struttura tridimensionale.
Nonostante l’ultrastruttura fine del DNA sia nota da oltre 70 anni, le strutture in vivo che sottendono reazioni fondamentali del metabolismo del DNA – come replicazione, riparazione, trascrizione e ricombinazione – restano in gran parte sconosciute. Anche le strutture specifiche dei cromosomi, tra cui centromeri, telomeri, sequenze ripetitive (es. DNA satellite) e elementi extracromosomici come i cerchi di DNA e il DNA mitocondriale, presentano ancora aspetti strutturali in vivo poco chiari.
Una regolazione precisa di questi processi, e delle loro interazioni, è essenziale per mantenere la stabilità genomica e prevenire l’insorgenza di mutazioni e alterazioni cromosomiche, elementi chiave nella genesi dei tumori.
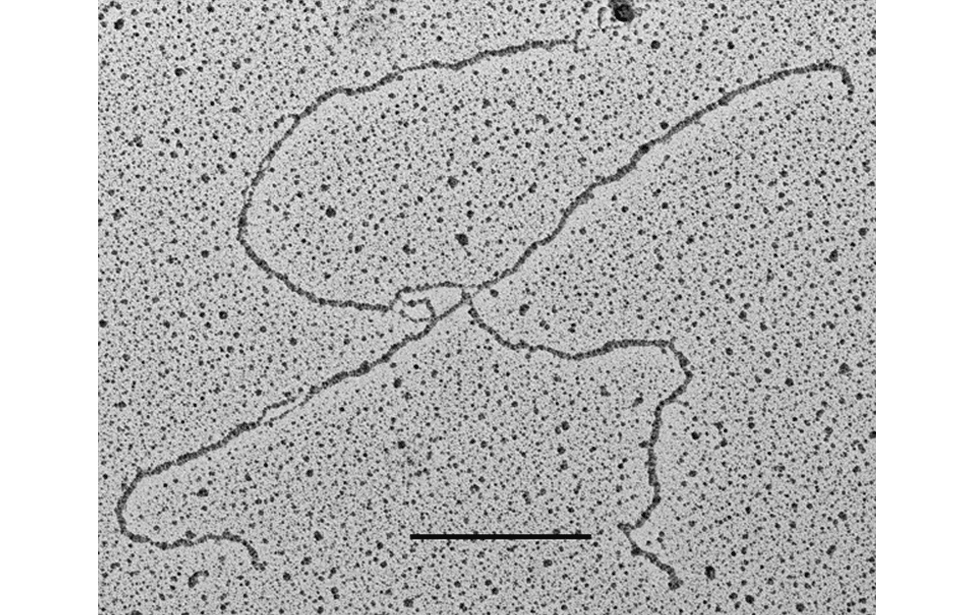
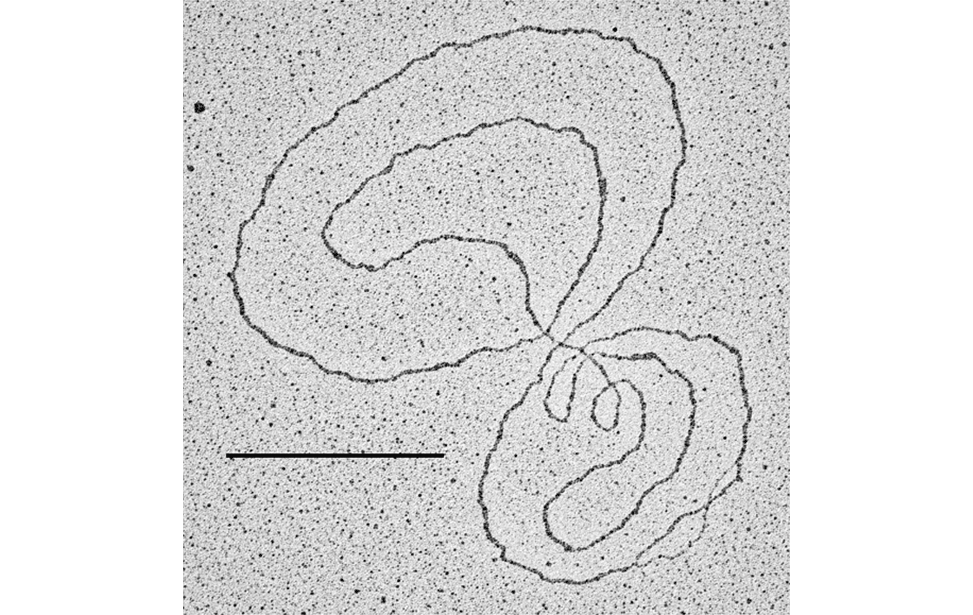
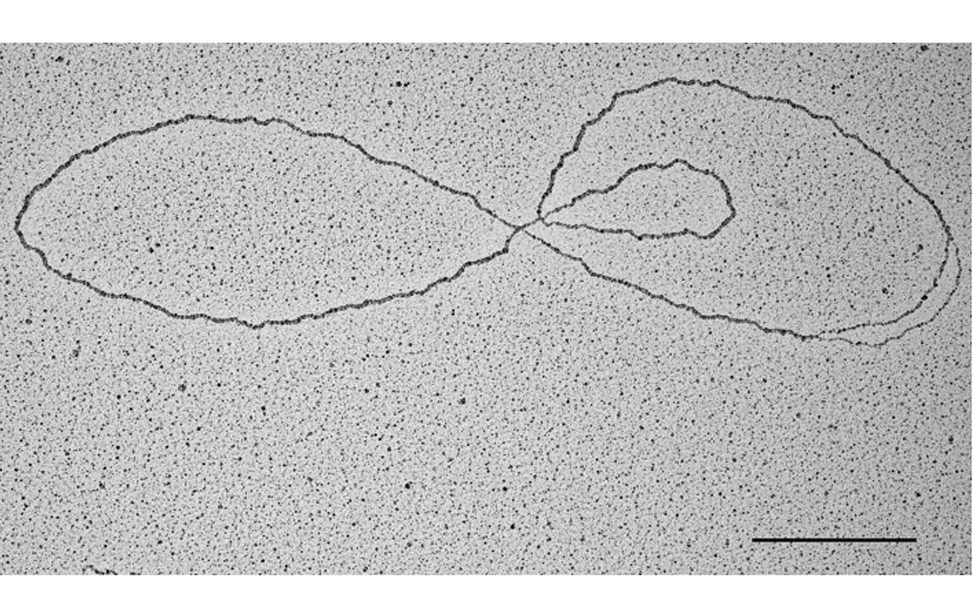
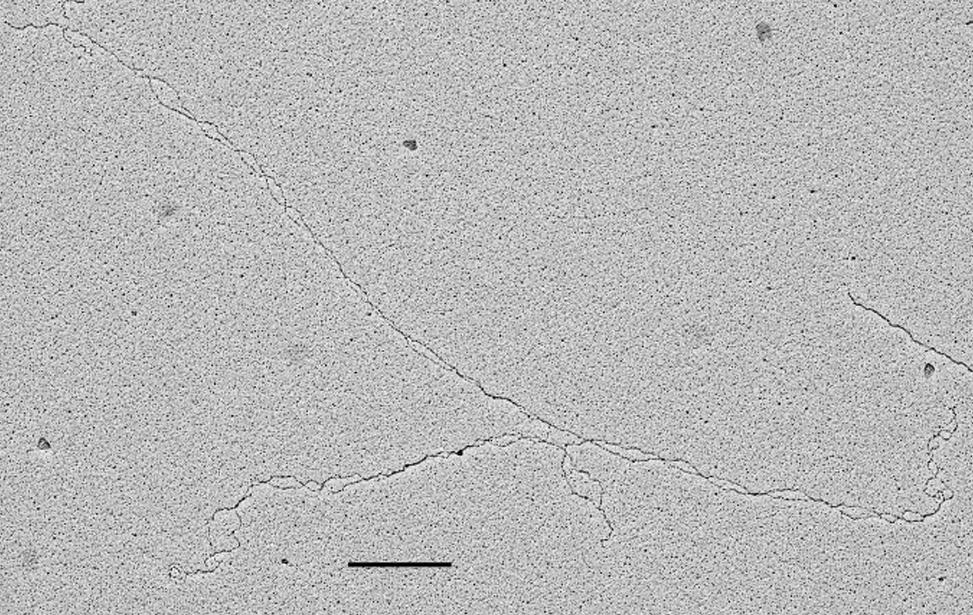
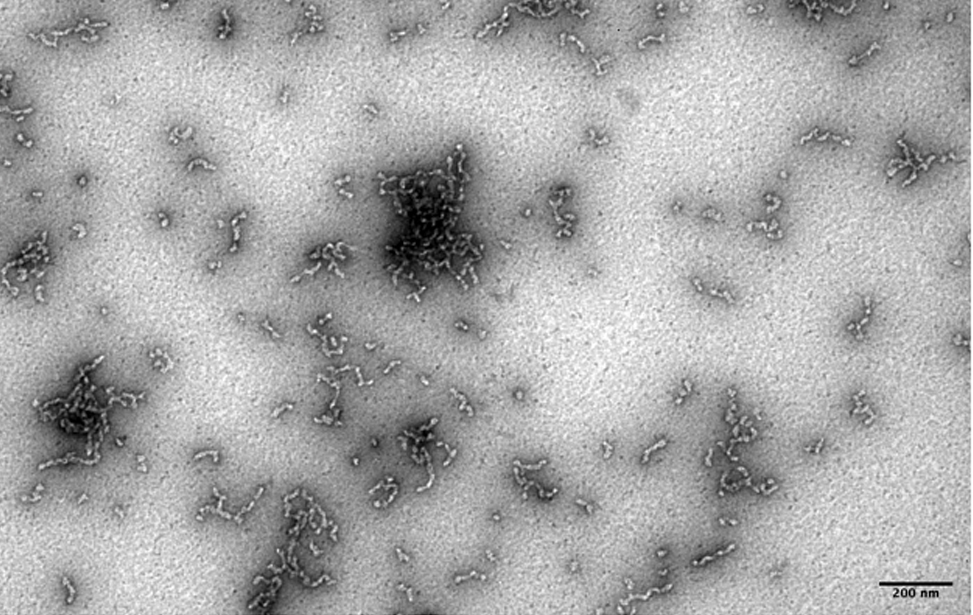
La piattaforma utilizza la tecnica del rotary shadowing in combinazione con TEM per analizzare strutture di DNA in vivo, una volta che sono state adeguatamente purificate ed arricchite rispetto al DNA lineare non informativo.
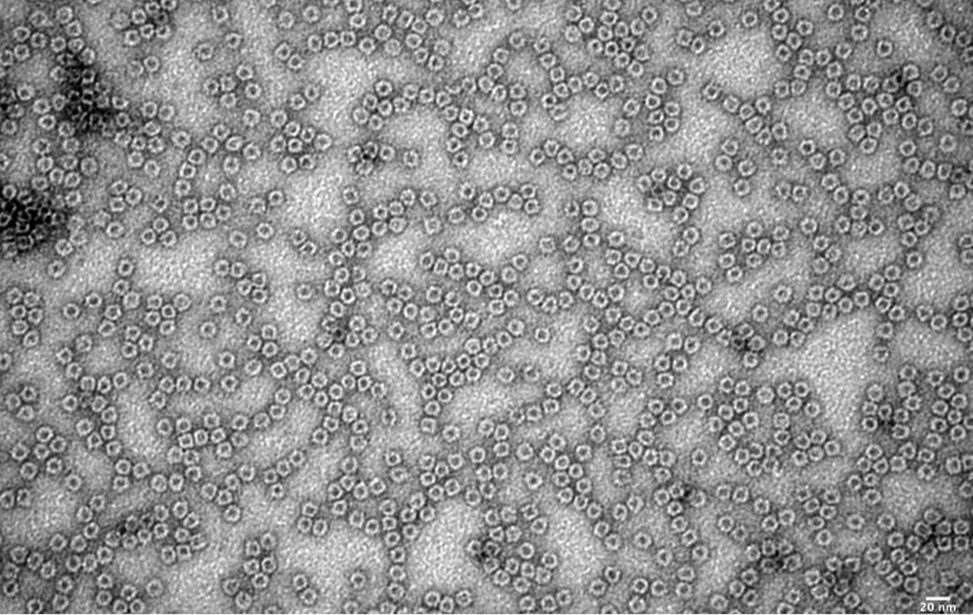
La facility studia anche la struttura delle proteine mediante negative staining e rotary shadowing e, a breve, sarà introdotta anche la cryo-microscopia elettronica (Cryo-EM) per l’osservazione di acidi nucleici e proteine nel loro stato nativo. Oggetto di studio sono anche protofibrille e fibrille associate a malattie e tumori, aggregati da misfolding proteico e strutture di complessi DNA-proteina.
La piattaforma offre attività di formazione per ricercatori, abilitandoli all’uso di tecniche TEM complesse applicate allo studio di singole molecole. Attraverso un approccio collaborativo con i gruppi di ricerca IFOM, contribuisce allo sviluppo continuo di nuovi metodi per lo studio delle strutture del DNA in vivo e dei complessi sovramolecolari proteici e DNA-proteina, sia in condizioni fisiologiche che patologiche.
La piattaforma EMSM supporta progetti di ricerca attraverso tecniche TEM ad alta risoluzione e imaging tridimensionale per la visualizzazione di acidi nucleici, proteine e complessi proteina-acido nucleico. Le principali applicazioni includono:
Analisi strutturale di DNA e RNA
- Visualizzazione della struttura in vivo del DNA cromosomico e dei complessi DNA-RNA coinvolti in replicazione, riparazione, ricombinazione e trascrizione.
- Studio delle strutture in vivo di elementi cromosomici ripetitivi come centromeri, telomeri e DNA satellite.
- Caratterizzazione strutturale di DNA episomico, come cerchi di DNA extracromosomici e intermedi della replicazione del DNA mitocondriale.
Instabilità genomica e ricerca sul cancro
- Identificazione di strutture di acidi nucleici associate a patologie tumorali.
- Analisi ultrastrutturale di DNA, RNA e intermedi DNA-RNA per applicazioni potenzialmente diagnostiche.
Proteine e complessi DNA-proteina
- Visualizzazione di singole proteine e complessi DNA-proteina tramite negative staining e rotary shadowing.
- Studio strutturale di protofibrille, fibrille e assemblaggi sovramolecolari in cellule sane e patologiche.
- Media di classi 2D e ricostruzioni 3D a bassa risoluzione di strutture proteiche e complessi DNA-proteina da dataset TEM.
Formazione e rete di utenti
- Formazione dei ricercatori IFOM all’uso di tecniche avanzate di microscopia elettronica a singola molecola.
- Sviluppo di una rete di utenti competenti nell’utilizzo della microscopia elettronica a singola particella e nell’innovazione metodologica.
La facility collabora attivamente con i gruppi di ricerca IFOM, tra cui quelli guidati da Dana Branzei, Vincenzo Costanzo, Fabrizio d’Adda di Fagagna, Ylli Doksani, Marco Foiani, Angela Bachi e Simona Polo. Queste collaborazioni sono parte integrante della strategia di ricerca Athena di IFOM, dedicata allo studio dell’integrità genomica e della biologia del cancro.
La facility EMSM è dotata di strumentazione avanzata per lo studio dell’ultrastruttura e delle interazioni molecolari tramite microscopia elettronica. Include:
- Microscopio elettronico a trasmissione Thermo Fisher TALOS F200C G2
Microscopio TEM da 200 kV di ultima generazione, equipaggiato con Cryo box, camera Ceta-S e software MAPS, Tomography, EPU e inspec3D. Permette l’analisi dell’ultrastruttura fine e della struttura tridimensionale di tessuti, cellule e biomolecole, sia a temperatura ambiente che nel loro stato nativo in ghiaccio vitreo. - Sistema Cryo Holder Gatan 626 con stazione di trasferimento cryo
Sistema Cryo Holder Gatan 626 con stazione di trasferimento cryo Comprende il portacampioni cryo a inclinazione singola Gatan 626, stazione di pompaggio turbo Gatan 655, controller di temperatura e stazione completa di trasferimento del campione criogenico. Strumento indispensabile per l’acquisizione di immagini in Cryo-EM, consente l’analisi di singole particelle, molecole, cellule e tessuti congelati. - Portacampioni per tomografia Fischione modello 2020
Essenziale per acquisire tomogrammi ad alta risoluzione per la ricostruzione tridimensionale di biomolecole, cellule e tessuti a temperatura ambiente. - Quorum GloQube Plus – Glow Discharger
Sistema per il trattamento superficiale dei supporti per TEM, fondamentale per garantire una distribuzione uniforme dei campioni biologici. - Microscopio elettronico a trasmissione FEI Tecnai 12 G2 Biotwin
Microscopio TEM entry-level dotato di camera laterale Gatan Orius SC-1000. Utilizzato per il controllo qualità dei campioni, lo screening e la formazione di utenti alle prime esperienze con la microscopia elettronica. - Evaporatore a fascio elettronico Leica ACE600
Macchina completamente automatizzata di nuova generazione per la deposizione di sottili strati metallici di alta qualità. Questi strati metallici (nell’ordine di qualche nanometro di spessore), sono necessari sia per la preparazione di tutti i tipi di supporti per i campioni di microscopia elettronica che, in particolare, per la tecnica del rotary shadowing per la visualizzazione di acidi nucleici. - Evaporatore a fascio elettronico Leica MED020
Composto da monitor QSG100, due cannoni E-beam e unità EVM030. Utilizzato per la deposizione di strati sottili di carbonio (ed altri metalli) di alta qualità, necessari alla preparazione dei supporti per i campioni, in particolare per la tecnica rotary shadowing su acidi nucleici.
Ringraziamenti alla Facility
In base alle Core Facilities Guidelines, qualora i servizi di una Facility siano stati utilizzati in un lavoro descritto in una pubblicazione, la Facility deve essere citata nei ringraziamenti, indicando sia il nome della Facility sia il relativo Research Resource Identifier (RRID).
Esempio di ringraziamento:
Il lavoro descritto è stato supportato dalla IFOM Microscopia elettronica a singole molecole Core Facility (RRID: SCR_026864).
Co‑Authorship
Se un membro dello staff di una Core Facility IFOM o Cogentech contribuisce in modo sostanziale a un lavoro pubblicato, deve essere incluso come co‑autore.
Ulteriori informazioni sono disponibili nelle sezioni Recommended guidelines e Acknowledging and citing core facilities
Esempi di contributi sostanziali che possono giustificare la co‑autorship includono:
- Contributo alla progettazione sperimentale o all’ottimizzazione degli esperimenti
- Sviluppo o adattamento significativo di metodi o protocolli
- Analisi avanzata e interpretazione dei dati
- Contributo intellettuale che ha influenzato la direzione scientifica dello studio
Il supporto tecnico di routine o l’erogazione di servizi standard, di norma, giustificano il solo ringraziamento e non la co‑autorship.
- Oxidative stress at telomeres triggers internal DNA loops, TRF1 dissociation, and TRF2-dependent R-loops
Nguyen TT, Mazzucco G, Kyriacou E, Lunardi T, Brandl L, Ahmed W, Doksani Y, Lingner J.
Nucleic Acids Res. 2025 Apr 10;53(7):gkaf285. doi: 10.1093/nar/gkaf285. PMID: 40219969 - HMCES corrupts replication fork stability during base excision repair in homologous recombination-deficient cells
Peña-Gómez MJ, Rodríguez-Martín Y, Del Rio Oliva M, Wijesekara Hanthi Y, Berrada S, Freire R, Masson JY, Reyes JC, Costanzo V, Rosado IV.
Sci Adv. 2025 Mar 28;11(13):eads3227. doi: 10.1126/sciadv.ads3227. Epub 2025 Mar 26.PMID: 40138423 - RAD51 protects abasic sites to prevent replication fork breakage
Hanthi YW, Ramirez-Otero MA, Appleby R, De Antoni A, Joudeh L, Sannino V, Waked S, Ardizzoia A, Barra V, Fachinetti D, Pellegrini L, Costanzo V. Mol Cell. 2024 Aug 22;84(16):3026-3043.e11. doi: 10.1016/j.molcel.2024.07.004. PMID: 39178838 Free article. - Unveiling the mechanistic link between extracellular amyloid fibrils, mechano-signaling and YAP activation in cancer.
Farris F, Elhagh A, Vigorito I, Alongi N, Pisati F, Giannattasio M, Casagrande F, Veghini L, Corbo V, Tripodo C, Di Napoli A, Matafora V, Bachi A. Cell Death Dis. 2024 Jan 11;15(1):28. doi: 10.1038/s41419-024-06424-z. PMID: 38199984 Free PMC article. - Sen1 and Rrm3 ensure permissive topological conditions for replication termination
Ramveer Choudhary, Joanna Niska-Blakie, Mohamood Adhil, Giordano Liberi, Yathish Jagadheesh Achar, Michele Giannattasio, Marco Foiani.
Cell Rep. 2023 Jul 4;42(7):112747. doi: 10.1016/j.celrep.2023.112747. - RFWD3 promotes ZRANB3 recruitment to regulate the remodeling of stalled replication forks.
Moore CE, Yalcindag SE, Czeladko H, Ravindranathan R, Wijesekara Hanthi Y, Levy JC, Sannino V, Schindler D, Ciccia A, Costanzo V, Elia AEH.
J Cell Biol. 2023 May 1;222(5):e202106022. doi: 10.1083/jcb.202106022. Epub 2023 Apr 10. PMID: 37036693 - The telomerase reverse transcriptase elongates reversed replication forks at telomeric repeats.
Huda A, Arakawa H, Mazzucco G, Galli M, Petrocelli V, Casola S, Chen L, Doksani Y.
Sci Adv. 2023 Mar 22;9(12):eadf2011. doi: 10.1126/sciadv.adf2011. Epub 2023 Mar 22. PMID: 36947627 Free PMC article. - Short-term molecular consequences of chromosome mis-segregation for genome stability
Lorenza Garribba , Giuseppina De Feudis , Valentino Martis , Martina Galli , Marie Dumont , Yonatan Eliezer , René Wardenaar , Marica Rosaria Ippolito, Divya Ramalingam Iyer, Andréa E Tijhuis , Diana C J Spierings , Michael Schubert , Silvia Taglietti , Chiara Soriani , Simon Gemble , Renata Basto , Nick Rhind , Floris Foijer , Uri Ben-David , Daniele Fachinetti , Ylli Doksani , Stefano Santaguida
Nat Commun . 2023 Mar 11;14(1):1353. doi: 10.1038/s41467-023-37095-7. - Enrichment of DNA replication intermediates by EdU pull down
Pessina, F., Romussi, A., Piccini, D., Mazzucco, G, Varasi, M., and Doksani, Y. (2022)
Methods in Cell Biology. Book Chapter - POLq prevents MRE11-NBS1-CtIP dependent fork breakage in the absence of BRCA2/RAD51 by filling lagging strand gaps.
Anjali Mann, Miguel Angel Ramirez-Otero, Anna De Antoni, Yodhara WijesekaraHanthi, Vincenzo Sannino, Giorgio Baldi, Lucia Falbo, Anna Schrempf, Sara Bernardo, Joanna Loizou, Vincenzo Costanzo.
Mol Cell 2022. Volume 82, Issue 22,2022,Pages 4218-4231.e8,ISSN 1097-2765, https://doi.org/10.1016/j.molcel.2022.09.013. - Rad51-mediated replication of damaged templates relies on monoSUMOylated DDK kinase
Chinnu Rose Joseph, Sabrina Dusi, Michele Giannattasio, Dana Branzei
Nat Commun 2022. May 5;13(1):2480. doi: 10.1038/s41467-022-30215-9. - Parental histone deposition on the replicated strands promotes error-free DNA damage tolerance and regulates drug resistance
Valeria Dolce, Sabrina Dusi, Michele Giannattasio, Chinnu Rose Joseph, Marco Fumasoni, Dana Branzei
Genes Dev 2022. Feb 1;36(3-4):167-179. doi: 10.1101/gad.349207.121. Epub 2022 Feb 3. - A rapid method to visualize human mitochondrial DNA replication through rotary shadowing and transmission electron microscopy
Martin Kosar, Daniele Piccini, Marco Foiani, Michele Giannattasio
Nucleic Acids Research, Volume 49, Issue 21, 2 December 2021, Page e121, https://doi.org/10.1093/nar/gkab770 - REV1-Polζ maintains the viability of homologous recombination-deficient cancer cells through mutagenic repair of PRIMPOL-dependent ssDNA gaps
Angelo Taglialatela, Giuseppe Leuzzi , Vincenzo Sannino , Raquel Cuella-Martin , Jen-Wei Huang , Foon Wu-Baer , Richard Baer , Vincenzo Costanzo , Alberto Ciccia.
Mol Cell. 2021 Oct 7;81(19):4008-4025.e7. doi: 10.1016/j.molcel.2021.08.016. - Checkpoint-mediated DNA polymerase ε exonuclease activity curbing counteracts resection-driven fork collapse.
Grazia Pellicanò, Mohammed Al Mamun, Dolores Jurado-Santiago , Sara Villa-Hernández , Xingyu Yin , Michele Giannattasio , Michael C Lanz , Marcus B Smolka , Joseph Yeeles , Katsuhiko Shirahige, Miguel García-Díaz , Rodrigo Bermejo
Mol Cell. 2021 Jul 1;81(13):2778-2792.e4. doi: 10.1016/j.molcel.2021.04.006. Epub 2021 Apr 30 - Smc5/6 functions with Sgs1-Top3-Rmi1 to complete chromosome replication at natural pause sites.
Sumedha Agashe , Chinnu Rose Joseph , Teresa Anne Clarisse Reyes , Demis Menolfi , Michele Giannattasio , Anja Waizenegger , Barnabas Szakal , Dana Branzei
Nat Commun. 2021 Apr 8;12(1):2111. doi: 10.1038/s41467-021-22217-w. - The human nucleoporin Tpr protects cells from RNA-mediated replication stress.
Martin Kosar , Michele Giannattasio , Daniele Piccini , Apolinar Maya-Mendoza , Francisco García-Benítez , Jirina Bartkova , Sonia I Barroso , Hélène Gaillard , Emanuele Martini, Umberto Restuccia , Miguel Angel Ramirez-Otero, Massimiliano Garre, Eleonora Verga, Miguel Andújar-Sánchez , Scott Maynard , Zdenek Hodny , Vincenzo Costanzo , Amit Kumar , Angela Bachi , Andrés Aguilera , Jiri Bartek , Marco Foiani
Nat Commun.2021 Jun 24;12(1):3937. doi: 10.1038/s41467-021-24224-3. - Telomere damage induces internal loops that generate telomeric circles.
Giulia Mazzucco, Armela Huda, Martina Galli, Daniele Piccini, Michele Giannattasio, Fabio Pessina, Ylli Doksani
Nat Commun. 2020 Oct 20;11(1):5297. doi: 10.1038/s41467-020-19139-4. - Physiological Tolerance to ssDNA Enables Strand Uncoupling during DNA Replication.
Amaia Ercilla, Jan Benada , Sampath Amitash, Gijs Zonderland, Giorgio Baldi , Kumar Somyajit, Fena Ochs ,Vincenzo Costanzo , Jiri Lukas ,Luis Toledo
Cell Rep 2020 Feb 18;30(7):2416-2429. doi: 10.1016/j.celrep.2020.01.067
- Dna2 processes behind the fork long ssDNA flaps generated by Pif1 and replication-dependent strand displacement.
Rossi SE, Foiani M, Giannattasio M.
Nature Communications. 2018 Nov 16;9(1):4830. doi: 10.1038/s41467-018-07378-5. - AND-1 fork protection function prevents fork resection and is essential for proliferation.
Abe T, Kawasumi R, Giannattasio M, Dusi S, Yoshimoto Y, Miyata K, Umemura K, Hirota K, Branzei D.
Nature Communications. 2018 Aug 6;9(1):3091. doi: 10.1038/s41467-018-05586-7. - Restoration of Replication Fork Stability in BRCA1- and BRCA2-Deficient Cells by Inactivation of SNF2-Family Fork Remodelers.
Taglialatela A, Alvarez S, Leuzzi G, Sannino V, Ranjha L, Huang JW, Madubata C, Anand R, Levy B, Rabadan R, Cejka P, Costanzo V, Ciccia A.
Molecular Cell. 2017 Oct 19;68(2):414-430.e8. doi: 10.1016/j.molcel.2017.09.036. - Fanconi-Anemia-Associated Mutations Destabilize RAD51 Filaments and Impair Replication Fork Protection.
Karina Zadorozhny, Vincenzo Sannino, Ondrej Beláň, Jarmila Mlčoušková, Mário Špírek, Vincenzo Costanzo, Lumír Krejčí.
Cell Rep 2017 Oct 10;21(2):333-340. doi: 10.1016/j.celrep. 2017.09.062. - Smarcal1-Mediated Fork Reversal Triggers Mre11-Dependent Degradation of Nascent DNA in the Absence of Brca2 and Stable Rad51 Nucleofilaments.
Kolinjivadi AM, Sannino V, De Antoni A, Zadorozhny K, Kilkenny M, Técher H, Baldi G, Shen R, Ciccia A, Pellegrini L, Krejci L, Costanzo V.
Molecular Cell. 2017 Sep 7;67(5):867-881.e7. doi: 10.1016/j.molcel.2017.07.001. Epub 2017 Jul 27. - Xenopus laevis as Model System to Study DNA Damage Response and Replication Fork Stability
Vincenzo Sannino , Federica Pezzimenti , Stefania Bertora , Vincenzo Costanzo. (2017)
Methods Enzymol. 2017;591:211-232. doi: 10.1016/bs.mie.2017.03.018. Epub 2017 Apr 8. - Centromeric DNA replication reconstitution reveals DNA loops and ATR checkpoint suppression.
Aze A, Sannino V, Soffientini P, Bachi A, Costanzo V.
Nature Cellular Biology. 2016 Jun;18(6):684-91. doi: 10.1038/ncb3344. Epub 2016 Apr 25. - Rad53-Mediated Regulation of Rrm3 and Pif1 DNA Helicases Contributes to Prevention of Aberrant Fork Transitions under Replication Stress.
Rossi SE, Ajazi A, Carotenuto W, Foiani M, Giannattasio M.
Cell Reports. 2015 Oct 6;13(1):80-92. doi: 10.1016/j.celrep.2015.08.073. Epub 2015 Sep 24. - Error-free DNA damage tolerance and sister chromatid proximity during DNA replication rely on the Polα/Primase/Ctf4 Complex.
Fumasoni M, Zwicky K, Vanoli F, Lopes M, Branzei D.
Molecular Cell. 2015 Mar 5;57(5):812-823. doi: 10.1016/j.molcel.2014.12.038. Epub 2015 Feb 5. - Visualization of recombination-mediated damage bypass by template switching.
Giannattasio M, Zwicky K, Follonier C, Foiani M, Lopes M, Branzei D.
Nature Structural & Molecular Biology. 2014 Oct;21(10):884-92. doi: 10.1038/nsmb.2888. Epub 2014 Sep 7.
DNA
Proteine
Strumentazione

Michele Giannattasio
Michele Giannattasio è biologo molecolare e genetista con competenze approfondite nell’uso della microscopia elettronica a trasmissione (TEM) per l’analisi strutturale di DNA, RNA e proteine. Ha conseguito la laurea magistrale in Biologia Molecolare (1998) e il dottorato in Genetica (2002) presso l’Università degli Studi di Milano, dove attualmente è anche ricercatore presso il Dipartimento di Oncologia ed Emato-Oncologia.
L’interesse per la TEM è iniziato nel 2008, con lo studio delle regioni a singolo filamento di DNA (ssDNA) generate durante la riparazione per escissione di nucleotidi (NER). Nel 2010 è entrato in IFOM come staff scientist, dedicandosi allo sviluppo di tecnologie TEM per la visualizzazione degli intermedi strutturali del DNA.
Ha collaborato con numerosi gruppi di ricerca IFOM, contribuendo in modo significativo allo studio dei meccanismi di tolleranza al danno del DNA, replicazione, ricombinazione e riparazione, sia in cellule sane che patologiche.
Ha svolto attività di ricerca presso il Centro di Microscopia Elettronica dell’Università di Zurigo e l’Istituto di Ricerca sul Cancro Molecolare della stessa città, specializzandosi in metodologie avanzate TEM e tecniche di preparazione dei campioni.
Dal 2017 è responsabile della piattaforma EMSM di IFOM, dove continua a promuovere l’utilizzo della microscopia elettronica per lo studio dell’ultrastruttura del genoma e delle proteine, rendendo queste competenze disponibili alla comunità scientifica IFOM